
|
PROPIEDADES DE LAS PROTEÍNAS Desde el punto de vista bioquímico, las propiedades de las proteínas son:
|
 |
PRECIPITACIÓN SELECTIVA DE LAS PROTEÍNAS
  El
agua es el disolvente biológico por excelencia. En disolución acuosa, los
residuos hidrofóbicos de las proteínas se acumulan en el interior
de la estructura, mientras que en la superficie aparecen diversos
grupos con carga eléctrica, en función del pH del medio (Figura de
la izquierda). En torno a los grupos cargados, los dipolos del agua se orientan
conforme a la carga eléctrica de cada grupo, de tal manera que la proteína
presenta una capa de solvatación formada por el agua de hidratación,
que es el agua retenida por las cargas eléctricas de la superficie de las
proteínas (En color rojo en la Figura superior derecha). Los AA polares
sin carga también se disponen en la superficie, donde interaccionan con
el agua mediante puentes de hidrógeno (Figura superior izquierda). El
agua es el disolvente biológico por excelencia. En disolución acuosa, los
residuos hidrofóbicos de las proteínas se acumulan en el interior
de la estructura, mientras que en la superficie aparecen diversos
grupos con carga eléctrica, en función del pH del medio (Figura de
la izquierda). En torno a los grupos cargados, los dipolos del agua se orientan
conforme a la carga eléctrica de cada grupo, de tal manera que la proteína
presenta una capa de solvatación formada por el agua de hidratación,
que es el agua retenida por las cargas eléctricas de la superficie de las
proteínas (En color rojo en la Figura superior derecha). Los AA polares
sin carga también se disponen en la superficie, donde interaccionan con
el agua mediante puentes de hidrógeno (Figura superior izquierda). |
|
Cualquier factor que modifique la interacción de la proteína con el disolvente disminuirá su estabilidad en disolución y provocará la precipitación. Así, la desaparición total o parcial de la envoltura acuosa, la neutralización de las cargas eléctricas de tipo repulsivo o la ruptura de los puentes de hidrógeno facilitará la agregación intermolecular y provocará la precipitación. La precipitación suele ser consecuencia del fenómeno llamado desnaturalización. Se llama desnaturalización de las proteínas a la pérdida de las estructuras de orden superior (secundaria, terciaria y cuaternaria), quedando la cadena polipeptídica reducida a un polímero estadístico sin ninguna estructura tridimensional fija (Figura inferior).
|
|
Cuando la proteína no ha sufrido ningún cambio en su interacción con el disolvente, se dice que presenta una estructura nativa. Cualquier alteración de la estructura nativa que modifique su interacción con el disolvente y que provoque su precipitación dará lugar a una estructura desnaturalizada. En una proteína cualquiera, la estructura nativa y la desnaturalizada tan sólo tienen en común la estructura primaria, es decir, la secuencia de AA que la componen. Los demás niveles de organización estructural desaparecen en la estructura desnaturalizada. La desnaturalización provoca diversos efectos en la proteína:
|
|
|
|
Los agentes que provocan la desnaturalización de una proteína se llaman agentes desnaturalizantes. Se distinguen agentes físicos (calor) y químicos (detergentes, disolventes orgánicos, pH, fuerza iónica). Como en algunos casos el fenómeno de la desnaturalización es reversible, es posible precipitar proteínas de manera selectiva mediante cambios en:
|
EFECTO DE LA POLARIDAD DEL DISOLVENTE SOBRE LA ESTRUCTURA DE LAS PROTEÍNAS
|
La polaridad del disolvente disminuye cuando se le añaden sustancias menos polares que el agua como el etanol o la acetona. Con ello disminuye el grado de hidratación de los grupos iónicos superficiales de la molécula proteica, provocando la agregación y precipitación. Los disolventes orgánicos interaccionan con el interior hidrofóbico de las proteínas y desorganizan la estructura terciaria, provocando su desnaturalización y precipitación. La acción de los detergentes es similar a la de los disolventes orgánicos. |
EFECTO DE LA FUERZA IÓNICA SOBRE LA ESTRUCTURA DE LAS PROTEÍNAS
|
Un aumento de la fuerza iónica del medio (por adición de sulfato amónico, urea o hidrocloruro de guanidinio, por ejemplo) también provoca una disminución en el grado de hidratación de los grupos iónicos superficiales de la proteína, ya que estos solutos (1) compiten por el agua y (2) rompen los puentes de hidrógeno o las interacciones electrostáticas, de forma que las moléculas proteicas se agregan y precipitan. En muchos casos, la precipitación provocada por el aumento de la fuerza iónica es reversible. Mediante una simple diálisis se puede eliminar el exceso de soluto y recuperar tanto la estructura como la función original. A veces es una disminución en la fuerza iónica la que provoca la precipitación. Así, las proteínas que se disuelven en medios salinos pueden desnaturalizarse al dializarlas frente a agua destilada, y se renaturalizan cuando se restaura la fuerza iónica original. |
EFECTO DEL pH SOBRE LA ESTRUCTURA DE LAS PROTEÍNAS
|
Los iones H+ y OH- del agua provocan efectos parecidos, pero además de afectar a la envoltura acuosa de las proteínas también afectan a la carga eléctrica de los grupos ácidos y básicos de las cadenas laterales de los aminoácidos. Esta alteración de la carga superficial de las proteínas elimina las interacciones electrostáticas que estabilizan la estructura terciaria y a menudo provoca su precipitación. La solubilidad de una proteína es mínima en su punto isoeléctrico, ya que su carga neta es cero y desaparece cualquier fuerza de repulsión electrostática que pudiera dificultar la formación de agregados. |
EFECTO DE LA TEMPERATURA SOBRE LA ESTRUCTURA DE LAS PROTEÍNAS
| Cuando la temperatura es elevada aumenta la energía cinética de las moléculas con lo que se desorganiza la envoltura acuosa de las proteínas, y se desnaturalizan. Asímismo, un aumento de la temperatura destruye las interacciones débiles y desorganiza la estructura de la proteína, de forma que el interior hidrofóbico interacciona con el medio acuoso y se produce la agregación y precipitación de la proteína desnaturalizada. |
CAPACIDAD AMORTIGUADORA DE LAS PROTEÍNAS
Esta propiedad se debe a la existencia de:
Por este motivo, las proteínas poseen un considerable poder amortiguador en una amplia zona de pH. Aunque cada AA tiene unos grupos ionizables con unas constantes de ionización (pKa) características, el valor de dichas constantes puede verse ligeramente modificado por el entorno proteico. El grupo imidazol del AA histidina es el principal responsable del poder amortiguador de las proteínas a pH fisiológico, ya que su pKa está próximo a 7. |
|||||||||||||||||||||||||||||||||
Cuando el pH es bajo, los grupos ionizables están protonados, y la carga neta de la proteína es de signo positivo. Cuando el pH es alto, los grupos ionizables están desprotonados, y la carga neta es de signo negativo. Entre ambas zonas, habrá un pH en el cual la carga neta de la proteína es nula. Es el pH isoeléctrico o punto isoeléctrico, y es característico de cada proteína (Tabla de la izquierda). A valores de pH por debajo del pH isoeléctrico la carga neta de la proteína es positiva, y a valores de pH por encima del pH isoeléctrico, la carga neta de la proteína es negativa. La mayoría de las proteínas intracelulares tienen carga negativa, ya que su pH isoeléctrico es menor que el pH fisiológico (que está proximo a 7). Se llaman proteínas ácidas a aquellas que tienen un punto isoeléctrico bajo (como la pepsina), y proteínas básicas a las que tienen un punto isoeléctrico alto (como las histonas). |
PROPIEDADES OSMÓTICAS DE LAS PROTEÍNAS
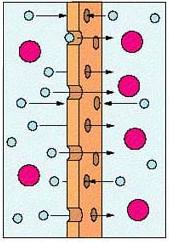 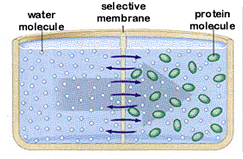 Como
todo soluto molecular o iónico, las proteínas ejercen un efecto osmótico
cuando existen barreras que limitan su libre difusión, como puede ser una
membrana semipermeable (Figura de la izquierda), que permite el paso
del agua, pero no de los solutos. Si tenemos dos compartimentos acuosos
separados por una membrana semipermeable y uno de ellos contiene proteínas,
éstas tienden a captar agua del compartimento vecino (Figura de la derecha).
Este efecto osmótico es proporcional al número de partículas
dispersas. El valor de la presión osmótica se puede calcular mediante la
fórmula de Van't Hoff: p
= cRT, donde p
es la presión osmótica, c es la concentración,
R es la constante de los gases y T es la temperatura
absoluta. Como
todo soluto molecular o iónico, las proteínas ejercen un efecto osmótico
cuando existen barreras que limitan su libre difusión, como puede ser una
membrana semipermeable (Figura de la izquierda), que permite el paso
del agua, pero no de los solutos. Si tenemos dos compartimentos acuosos
separados por una membrana semipermeable y uno de ellos contiene proteínas,
éstas tienden a captar agua del compartimento vecino (Figura de la derecha).
Este efecto osmótico es proporcional al número de partículas
dispersas. El valor de la presión osmótica se puede calcular mediante la
fórmula de Van't Hoff: p
= cRT, donde p
es la presión osmótica, c es la concentración,
R es la constante de los gases y T es la temperatura
absoluta. |
|
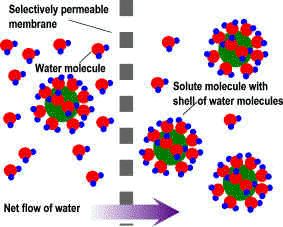
En el caso de las proteínas, el efecto osmótico se ve amplificado por otros dos factores. Por un lado, el agua de hidratación que forma la envoltura acuosa de las proteínas también contribuye a la presión osmótica (Figura de la derecha). |
|
 |
||||
|
Por otro lado, las proteínas se comportan como polianiones, cuyas cargas están neutralizadas por iones Na+ o K+ (Figura inferior izquierda). Las membranas biológicas son permeables a estos iones y a sus contraiones, con lo cual su concentración a ambos lados de la membrana se equilibra. Sin embargo, la existencia de proteínas en sólo uno de los compartimentos provoca la retención permanente de iones difusibles en ese lado de la membrana (efecto Donnan), lo que incrementa el efecto osmótico (Figura inferior derecha).
|
||||||
|
Se denomina presión coloidosmótica o presión oncótica al efecto osmótico conjunto de las proteínas, que es el resultado de:
|
|
|