|
Se define la unidad de actividad enzimática (U)
como la cantidad de enzima que cataliza la conversión de 1 µmol de sustrato
en un minuto. La actividad específica es el número de unidades de enzima
por miligramo de proteína (U/mg prot) o por mililitro de disolución (U/ml).
Recientemente, el Sistema Internacional de unidades (SI)
ha definido la unidad de actividad enzimática como la cantidad de enzima
que transforma 1 mol de sustrato por segundo. Esta unidad se llama katal
(kat). Como 1 mol son 106 µmoles y 1 minuto son 60 segundos,
resulta que 1 katal equivale a 60 x 106 U. Esta unidad es muy
grande, de forma que se utilizan frecuentemente los submúltiplos como
el microkatal (µkat, 10-6 kat) o el nanokatal (nkat, 10-9
kat).
Cuando se conoce el peso molecular del enzima puro y el
número de centros activos por molécula de enzima, las medidas de actividad
enzimática permiten calcular el número de recambio del enzima,
o sea, el número de reacciones elementales que realiza el enzima por cada
centro activo y por unidad de tiempo.
|
 Los
principios generales de las reacciones químicas se aplican también a las
reacciones enzimáticas. Por este motivo, antes de empezar con la cinética
química, se van a repasar algunos conceptos básicos
de cinética química.
Los
principios generales de las reacciones químicas se aplican también a las
reacciones enzimáticas. Por este motivo, antes de empezar con la cinética
química, se van a repasar algunos conceptos básicos
de cinética química.
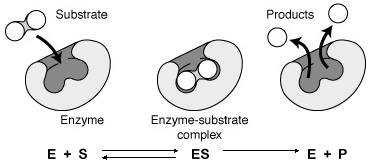 La
cinética enzimática estudia la velocidad de las reacciones catalizadas
por enzimas. Estos estudios proporcionan información directa acerca
del mecanismo de la reacción catalítica y de la especifidad del enzima.
La velocidad de una reacción catalizada por un enzima puede medirse con
relativa facilidad, ya que en muchos casos no es necesario purificar
o aislar el enzima. La medida se realiza siempre en las condiciones
óptimas de pH, temperatura, presencia de cofactores, etc, y se utilizan
concentraciones saturantes de sustrato. En estas condiciones, la velocidad
de reacción observada es la velocidad máxima (Vmax). La velocidad
puede determinarse bien midiendo la aparición de los productos o la desaparición
de los reactivos.
La
cinética enzimática estudia la velocidad de las reacciones catalizadas
por enzimas. Estos estudios proporcionan información directa acerca
del mecanismo de la reacción catalítica y de la especifidad del enzima.
La velocidad de una reacción catalizada por un enzima puede medirse con
relativa facilidad, ya que en muchos casos no es necesario purificar
o aislar el enzima. La medida se realiza siempre en las condiciones
óptimas de pH, temperatura, presencia de cofactores, etc, y se utilizan
concentraciones saturantes de sustrato. En estas condiciones, la velocidad
de reacción observada es la velocidad máxima (Vmax). La velocidad
puede determinarse bien midiendo la aparición de los productos o la desaparición
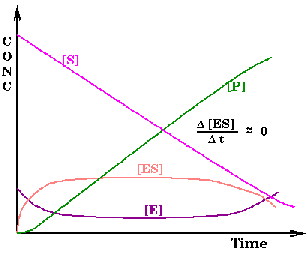
de los reactivos.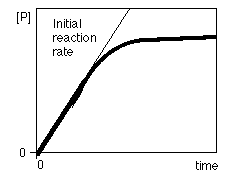 Al
seguir la velocidad de aparición de producto (o de desaparición del sustrato)
en función del tiempo se obtiene la llamada curva de avance de la reacción,
o simplemente, la cinética de la reacción. A medida que la reacción transcurre,
la velocidad de acumulación del producto va disminuyendo porque se va consumiendo
el sustrato de la reacción (Figura de la derecha).
Para evitar esta complicación se procede a medir la velocidad inicial
de la reacción (v0). La velocidad inicial de la reacción
es igual a la pendiente de la curva de avance a tiempo cero (Figura de la
derecha). De esta forma, la medida de v0 se realiza antes de
que se consuma el 10% del total del sustrato, de forma que pueda considerarse
la [S] como esencialmente constante a lo largo del experimento. Además,
en estas condiciones no es necesario considerar la reacción inversa,
ya que la cantidad de producto formada es tan pequeña que la reacción inversa
apenas ocurre. De esta forma se simplifican enormemente las ecuaciones de
velocidad.
Al
seguir la velocidad de aparición de producto (o de desaparición del sustrato)
en función del tiempo se obtiene la llamada curva de avance de la reacción,
o simplemente, la cinética de la reacción. A medida que la reacción transcurre,
la velocidad de acumulación del producto va disminuyendo porque se va consumiendo
el sustrato de la reacción (Figura de la derecha).
Para evitar esta complicación se procede a medir la velocidad inicial
de la reacción (v0). La velocidad inicial de la reacción
es igual a la pendiente de la curva de avance a tiempo cero (Figura de la
derecha). De esta forma, la medida de v0 se realiza antes de
que se consuma el 10% del total del sustrato, de forma que pueda considerarse
la [S] como esencialmente constante a lo largo del experimento. Además,
en estas condiciones no es necesario considerar la reacción inversa,
ya que la cantidad de producto formada es tan pequeña que la reacción inversa
apenas ocurre. De esta forma se simplifican enormemente las ecuaciones de
velocidad.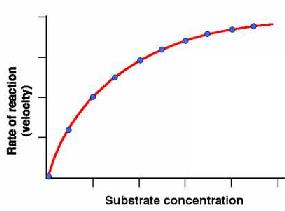 Para
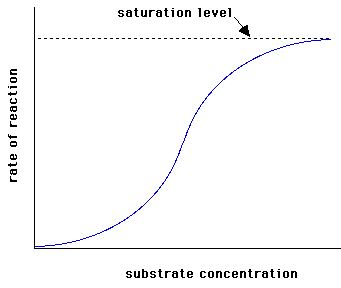
estudiar la cinética enzimática se mide el efecto de la concentración
inicial de sustrato sobre la velocidad inicial de la reacción, manteniendo
la cantidad de enzima constante. Si representamos v0 frente a
[S]0 obtenemos una gráfica como la de la Figura de la
derecha. Cuando [S]0 es pequeña, la velocidad inicial
es directamente proporcional a la concentración de sustrato, y por tanto,
la reacción es de primer orden. A altas [S]0, el
enzima se encuentra saturada por el sustrato, y la velocidad ya no depende
de [S]0. En este punto, la reacción es de orden cero y
la velocidad es máxima (Vmax).
Para
estudiar la cinética enzimática se mide el efecto de la concentración
inicial de sustrato sobre la velocidad inicial de la reacción, manteniendo
la cantidad de enzima constante. Si representamos v0 frente a
[S]0 obtenemos una gráfica como la de la Figura de la
derecha. Cuando [S]0 es pequeña, la velocidad inicial
es directamente proporcional a la concentración de sustrato, y por tanto,
la reacción es de primer orden. A altas [S]0, el
enzima se encuentra saturada por el sustrato, y la velocidad ya no depende
de [S]0. En este punto, la reacción es de orden cero y
la velocidad es máxima (Vmax).
 Los
estudios sistemáticos del efecto de la concentración inical del sustrato
sobre la actividad enzimática comenzaron a realizarse a finales del siglo
XIX. Ya en 1882 se introdujo el concepto del complejo enzima-sustrato
como intermediario del proceso de catálisis enzimática. En
1913, Leonor Michaelis (foto de la izquierda) y Maud Menten
(foto de la derecha) desarrollaron esta teoría y propusieron una
ecuación de velocidad que explica el comportamiento cinético de
los enzimas.
Los
estudios sistemáticos del efecto de la concentración inical del sustrato
sobre la actividad enzimática comenzaron a realizarse a finales del siglo
XIX. Ya en 1882 se introdujo el concepto del complejo enzima-sustrato
como intermediario del proceso de catálisis enzimática. En
1913, Leonor Michaelis (foto de la izquierda) y Maud Menten
(foto de la derecha) desarrollaron esta teoría y propusieron una
ecuación de velocidad que explica el comportamiento cinético de
los enzimas.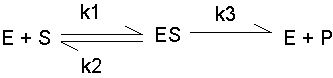
 Este
modelo cinético adopta la hipótesis del estado estacionario, según
la cual la concentración del complejo enzima-sustrato es pequeña
y constante a lo largo de la reacción (Figura de la derecha). Por
tanto, la velocidad de formación del complejo enzima-sustrato (v1)
es igual a la de su disociación (v2+ v3):
Este
modelo cinético adopta la hipótesis del estado estacionario, según
la cual la concentración del complejo enzima-sustrato es pequeña
y constante a lo largo de la reacción (Figura de la derecha). Por
tanto, la velocidad de formación del complejo enzima-sustrato (v1)
es igual a la de su disociación (v2+ v3): 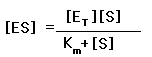 , siendo
, siendo 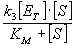
 Para
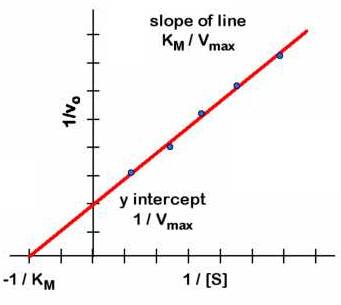
determinar gráficamente los valores de KM y Vmax
es más sencillo utilizar la representación doble recíproca (1/v0
frente a 1/[S]0), ya que es una línea recta. Esta representación
doble recíproca recibe el nombre de representación de Lineweaver-Burk
(Figura de la derecha). Es una recta en la cual:
Para
determinar gráficamente los valores de KM y Vmax
es más sencillo utilizar la representación doble recíproca (1/v0
frente a 1/[S]0), ya que es una línea recta. Esta representación
doble recíproca recibe el nombre de representación de Lineweaver-Burk
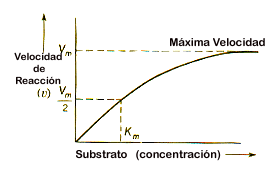
(Figura de la derecha). Es una recta en la cual: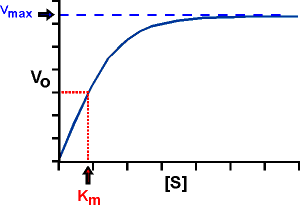 KM
es la concentración de sustrato para la cual la velocidad de reacción
es la mitad de la velocidad máxima. En efecto, si KM
= [S], la ecuación de Michaelis-Menten se reduce a: v = Vmax/2.
KM
es la concentración de sustrato para la cual la velocidad de reacción
es la mitad de la velocidad máxima. En efecto, si KM
= [S], la ecuación de Michaelis-Menten se reduce a: v = Vmax/2.
