|
Según este criterio, se distinguen los
siguientes grupos:
1.- NEUTROS O ALIFÁTICOS:
En ellos la cadena lateral es un hidrocarburo alifático. Son muy poco
reactivos, y fuertemente hidrofóbicos (excepto la Gly, cuya cadena
lateral es un átomo de hidrógeno). Estos AA hidrofóbicos tienden a
ocupar la parte central de las proteínas globulares, de modo que minimizan
su interacción con el disolvente. Pertenecen a este grupo: G, A, V,
L e I.
|
Glicina, Gly, G
|
Alanina, Ala, A
|
Valina, Val, V
|
Leucina, Leu, L
|
Isoleucina, Ile, I
|
|
|
|
|
|
|
2.- AROMÁTICOS: La cadena
lateral es un grupo aromático: benceno en el caso de la F, fenol en
el caso de la Y e indol en el caso del W. Estos AA, además de formar
parte de las proteínas son precursores de otras biomoléculas de interés:
hormonas tiroideas, pigmentos o neurotransmisores.
3.- HIDROXIÁMINOACIDOS:
Poseen un grupo alcohólico en su cadena lateral. Son la T y S.
|
Fenilalanina, Phe, F
|
Tirosina, Tyr, Y
|
Triptófano, Trp, W
|
Treonina, Thr, T
|
Serina, Ser, S
|
|
|
|
|
|
|
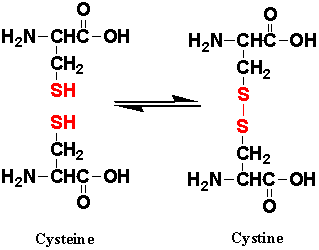
4.- TIOAMINOÁCIDOS:
Contienen azufre. Son C y M. La cisteína (C) tiene gran importancia
estructural en las proteínas porque puede reaccionar con el grupo
SH de otra C para formar un puente disulfuro (-S-S-), permitiendo
el plegamiento de la proteína. Por este motivo, en algunos hidrolizados
proteicos se obtiene el AA cistina, que está formado por dos
cisteínas unidas por un puente disulfuro.
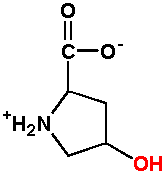
5.- IMINOÁCIDOS:
Tienen el grupo a-amino sustituído por
la propia cadena lateral, formando un anillo pirrolidínico. Es el
caso de la P.
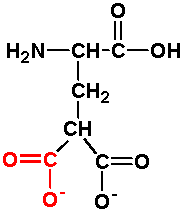
6.- DICARBOXÍLICOS
Y SUS AMIDAS: Son el ácido aspártico (D) y el ácido glutámico
(E). Sus amidas correspondientes son la asparragina (N) y la glutamina
(Q).
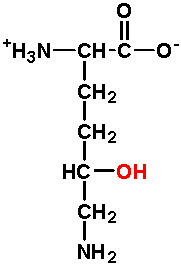
7.- DIBÁSICOS:
La cadena lateral contiene grupos básicos. El grupo básico puede ser
un grupo amino (K), un grupo guanidino (R) o un grupo imidazol (H).
|