 |
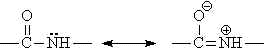 |
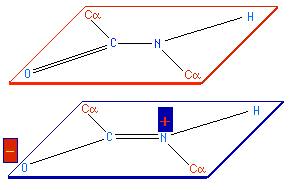
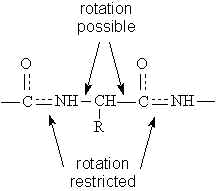
Los electrones p de los átomos de C, N y O no implicados en el enlace s pueden formar orbitales híbridos p. Como el N es menos electronegativo que el O, el enlace C-O tiene un 60% de carácter de doble enlace mientras que el enlace C-N tiene un 40%. Por lo tanto, se puede considerar que los enlaces C-O y N-C que participan en el enlace peptídico tienen estructuras intermedias entre el enlace sencillo y el enlace doble. Esta teoría se confirma por el hecho de que las distancias interatómicas medidas en el enlace C-O y en el enlace C-N son intermedias entre el enlace sencillo y el doble enlace. Esta disposición atómica está estabilizada por resonancia (Figura izquierda, abajo), de forma que los seis átomos implicados en la formación del enlace peptídico están contenidos en el mismo plano (Figura inferior izquierda).
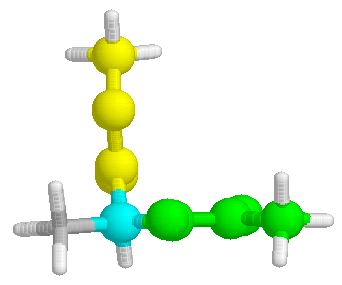
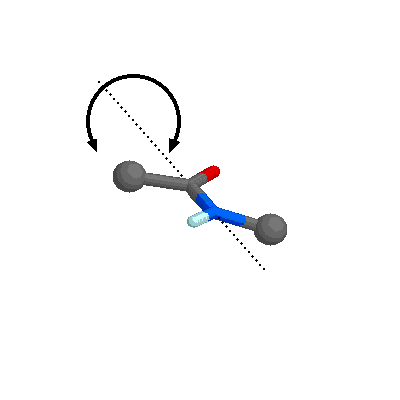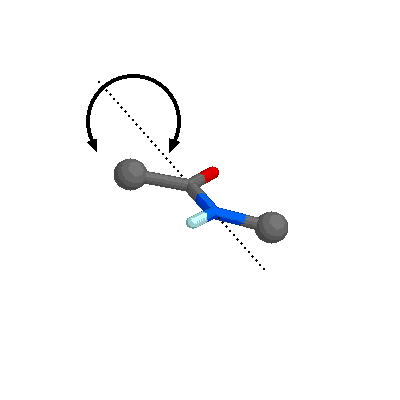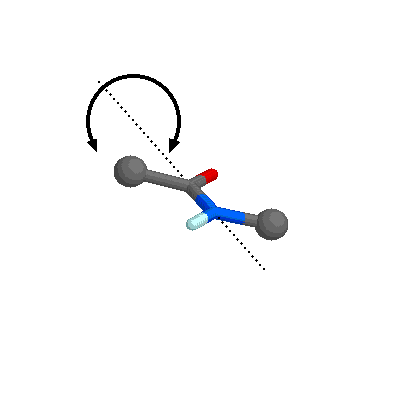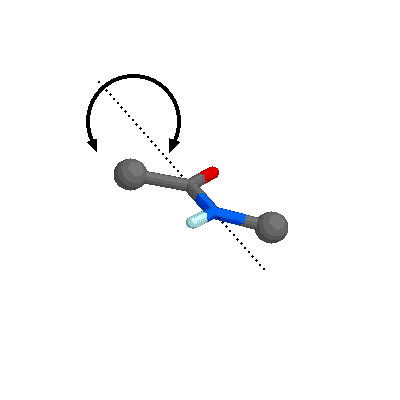

 El
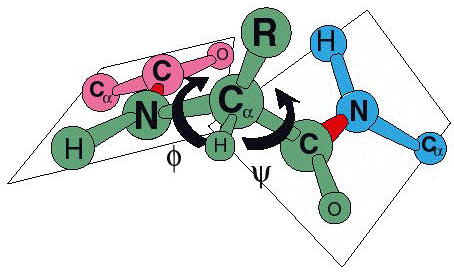
C2 (Ca) de cada AA implicado puede establecer
dos ángulos de torsión con los planos de los enlaces peptídicos contiguos:
los llamados ángulos f (phi) y y
(psi) (Figura de la derecha). El ángulo phi (f)
es la rotación del enlace N-Ca, y el ángulo
psi (y) la del enlace Ca-C.
En la estructura de un péptido o de una proteína, cada AA presenta un
valor de f y otro de y
determinados. Como estos son los únicos grados de libertad que presenta
la estructura, la conformación de la cadena polipéptídica queda completamente
determinada cuando se conocen los valores de y
y de f para cada AA.
El
C2 (Ca) de cada AA implicado puede establecer
dos ángulos de torsión con los planos de los enlaces peptídicos contiguos:
los llamados ángulos f (phi) y y
(psi) (Figura de la derecha). El ángulo phi (f)
es la rotación del enlace N-Ca, y el ángulo
psi (y) la del enlace Ca-C.
En la estructura de un péptido o de una proteína, cada AA presenta un
valor de f y otro de y
determinados. Como estos son los únicos grados de libertad que presenta
la estructura, la conformación de la cadena polipéptídica queda completamente
determinada cuando se conocen los valores de y
y de f para cada AA.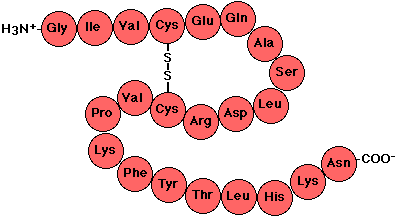 En
un extremo de la cadena polipeptídica queda un grupo amino libre (extremo
amino o extremo N-terminal) y en el extremo opuesto queda un carboxilo
libre (extremo carboxilo o extremo C terminal). Por convención,
los péptidos se nombran leyendo secuencialmente los radicales de los AA
que lo integran a partir del extremo N (Figura de la derecha). Se denomina
secuencia de un péptido al orden de los AA que lo integran. La
secuencia está determinada por dos factores:
En
un extremo de la cadena polipeptídica queda un grupo amino libre (extremo
amino o extremo N-terminal) y en el extremo opuesto queda un carboxilo
libre (extremo carboxilo o extremo C terminal). Por convención,
los péptidos se nombran leyendo secuencialmente los radicales de los AA
que lo integran a partir del extremo N (Figura de la derecha). Se denomina
secuencia de un péptido al orden de los AA que lo integran. La
secuencia está determinada por dos factores: