|
A veces, un enzima requiere para su función la presencia
de sustancias no proteicas que colaboran en la catálisis: los cofactores.
Los cofactores pueden ser iones inorgánicos como el Fe++, Mg++,
Mn++, Zn++ etc. Casi un tercio de los enzimas conocidos
requieren cofactores. Cuando el cofactor es una molécula orgánica se llama
coenzima. Muchos de estos coenzimas se sintetizan a partir de vitaminas.
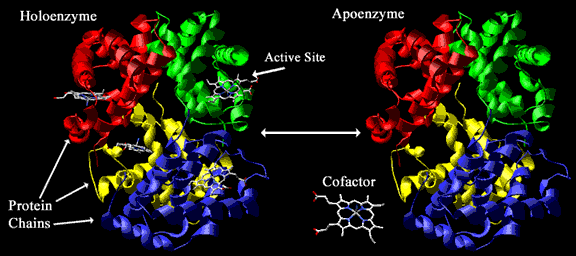
En la figura inferior podemos observar una molécula de hemoglobina
(proteína que transporta oxígeno) y su coenzima (el grupo
hemo). Cuando los cofactores y las coenzimas se encuentran unidos covalentemente
al enzima se llaman grupos prostéticos. La
forma catalíticamente activa del enzima, es decir, el enzima unida a su
grupo prostético, se llama holoenzima. La parte proteica de un
holoenzima (inactiva) se llama apoenzima, de forma que:
|
apoenzima + grupo prostético=
holoenzima
|
|
|
|
 Los
enzimas son proteínas que catalizan reacciones químicas en los seres
vivos. Los enzimas son catalizadores, es decir, sustancias que, sin consumirse
en una reacción, aumentan notablemente su velocidad. No hacen factibles
las reacciones imposibles, sino que sólamente aceleran las que espontáneamente
podrían producirse. Ello hace posible que en condiciones fisiológicas tengan
lugar reacciones que sin catalizador requerirían condiciones extremas de
presión, temperatura o pH.
Los
enzimas son proteínas que catalizan reacciones químicas en los seres
vivos. Los enzimas son catalizadores, es decir, sustancias que, sin consumirse
en una reacción, aumentan notablemente su velocidad. No hacen factibles
las reacciones imposibles, sino que sólamente aceleran las que espontáneamente
podrían producirse. Ello hace posible que en condiciones fisiológicas tengan
lugar reacciones que sin catalizador requerirían condiciones extremas de
presión, temperatura o pH.

 Los
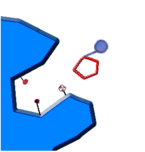
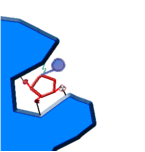
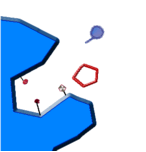
enzimas poseen grupos químicos ionizables (carboxilos -COOH; amino -NH2;
tiol -SH; imidazol, etc.) en las cadenas laterales de sus aminoácidos. Según
el pH del medio, estos grupos pueden tener carga eléctrica positiva, negativa
o neutra. Como la conformación de las proteínas depende, en parte, de sus
cargas eléctricas, habrá un pH en el cual la conformación será la más adecuada
para la actividad catalítica. Este es el llamado pH óptimo. (Para
activar la animación de la Figura de la derecha, pulsar la opción
"Recargar" del navegador).
Los
enzimas poseen grupos químicos ionizables (carboxilos -COOH; amino -NH2;
tiol -SH; imidazol, etc.) en las cadenas laterales de sus aminoácidos. Según
el pH del medio, estos grupos pueden tener carga eléctrica positiva, negativa
o neutra. Como la conformación de las proteínas depende, en parte, de sus
cargas eléctricas, habrá un pH en el cual la conformación será la más adecuada
para la actividad catalítica. Este es el llamado pH óptimo. (Para
activar la animación de la Figura de la derecha, pulsar la opción
"Recargar" del navegador).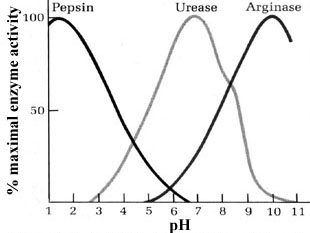 La
mayoría de los enzimas son muy sensibles a los cambios de pH. Desviaciones
de pocas décimas por encima o por debajo del pH óptimo pueden afectar drásticamente
su actividad. Así, la pepsina gástrica tiene un pH óptimo de 2, la ureasa
lo tiene a pH 7 y la arginasa lo tiene a pH 10 (Figura de la izquierda).
Como ligeros cambios del pH pueden provocar la desnaturalización de la proteína,
los seres vivos han desarrollado sistemas más o menos complejos para mantener
estable el pH intracelular: Los amortiguadores fisiológicos.
La
mayoría de los enzimas son muy sensibles a los cambios de pH. Desviaciones
de pocas décimas por encima o por debajo del pH óptimo pueden afectar drásticamente
su actividad. Así, la pepsina gástrica tiene un pH óptimo de 2, la ureasa
lo tiene a pH 7 y la arginasa lo tiene a pH 10 (Figura de la izquierda).
Como ligeros cambios del pH pueden provocar la desnaturalización de la proteína,
los seres vivos han desarrollado sistemas más o menos complejos para mantener
estable el pH intracelular: Los amortiguadores fisiológicos.
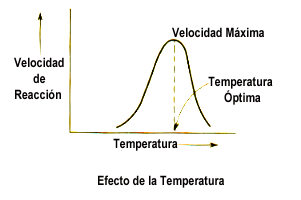 En
general, los aumentos de temperatura aceleran las reacciones químicas:
por cada 10ºC de incremento, la velocidad de reacción se duplica. Las
reacciones catalizadas por enzimas siguen esta ley general. Sin embargo,
al ser proteínas, a partir de cierta temperatura, se empiezan a desnaturalizar
por el calor. La temperatura a la cual la actividad catalítica es máxima
se llama temperatura óptima (Figura de la derecha). Por encima
de esta temperatura, el aumento de velocidad de la reacción debido a la
temperatura es contrarrestado por la pérdida de actividad catalítica debida
a la desnaturalización térmica, y la actividad enzimática decrece rápidamente
hasta anularse.
En
general, los aumentos de temperatura aceleran las reacciones químicas:
por cada 10ºC de incremento, la velocidad de reacción se duplica. Las
reacciones catalizadas por enzimas siguen esta ley general. Sin embargo,
al ser proteínas, a partir de cierta temperatura, se empiezan a desnaturalizar
por el calor. La temperatura a la cual la actividad catalítica es máxima
se llama temperatura óptima (Figura de la derecha). Por encima
de esta temperatura, el aumento de velocidad de la reacción debido a la
temperatura es contrarrestado por la pérdida de actividad catalítica debida
a la desnaturalización térmica, y la actividad enzimática decrece rápidamente
hasta anularse.